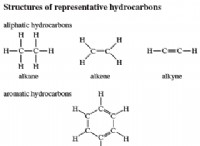
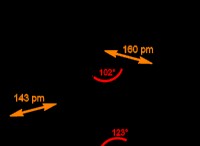
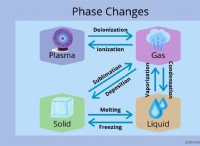
基本原理:電子がキーです
* 化学反応はすべて、電子の再配置に関するものです。 原子は、電子を共有または伝達して新しい結合を形成し、古い結合を壊し、最終的に異なる物質を作成することにより相互作用します。
変更の種類:
1。新しい絆の形成:
* 電子の共有: 2つの原子が電子を共有すると、共有結合が形成されます。 これにより、全体的なエネルギー状態が低い安定した配置が作成されます。
* 電子の伝達: イオン結合は、ある原子が電子を別の原子に寄付すると形成され、互いに引き付ける正に負の帯電イオンを作成します。
2。既存の債券の破壊:
* エネルギー入力: 既存の債券を破るにはエネルギーが必要です。 このエネルギーは、熱、光、さらには別の化学反応によって供給できます。
* 結合ブレイキングは電子を放出します: 結合が壊れると、関与する電子が共有または転送されなくなります。
3。再配置電子:
* 酸化還元反応: 多くの化学反応には、ある種から別の種への電子の移動が含まれます。これは酸化還元反応と呼ばれ、1つの種が酸化され(電子が失われます)、もう1種が還元されます(誘発電子)。
* その他の再配置: 電子の明確な伝達を伴わない反応でさえ、分子内の電子分布が変化します。これは、製品の反応性と特性に影響を与える可能性があります。
例:メタンの燃焼
* 反応物: メタン(CH4)と酸素(O2)
* 製品: 二酸化炭素(CO2)と水(H2O)
この反応で:
* 結合が壊れています: メタンと酸素の結合は壊れています。
* 電子が再配布されます: メタン中の炭素原子は、酸素原子を伴う電子を共有して二酸化炭素を形成し、メタンの水素原子は酸素原子を伴う電子を共有して水を形成します。
重要な考慮事項:
* 質量の保存: 各要素の原子の数は、反応全体で同じままです。 変化するのは電子の配置にすぎません。
* エネルギーの変化: 化学反応は、エネルギー(発熱)または吸収エネルギー(吸熱)を放出する可能性があります。 結合エネルギーの変化は、反応が発熱性であるか吸熱性かを決定します。
* 反応速度: 反応が発生する速度は、温度、濃度、触媒の存在などの要因に依存します。 これらの要因は、反応物分子間の衝突の頻度と結合を破壊する可能性に影響します。
本質的に、化学反応は電子の踊りを操作することです。古い債券を壊して新しいボンドを形成することにより、原子はより安定した構成を実現するために自分自身を再配置します。