五酸化リンの式は P4O10 で、白色の結晶性固体です。リン酸の無水物であるこの無機化合物は、無水リン酸、酸化リン (V)、五酸化二リン、十酸化四リン、および十酸化四リンとしても知られています。この化合物は吸湿性が高いため、強力な乾燥剤および脱水剤として利用されています。 b>
五酸化リンの構造:
五酸化リンが結晶化すると、少なくとも 4 つの多形が存在します。最もよく知られている準安定型は、P4O10 分子で構成されています。これらの分子は、弱いファン デル ワールス力によって六方格子にまとめられています (ただし、分子の対称性が高いにもかかわらず、結晶のパッキングは最密パッキングではありません)。 P4O10 ケージ構造は、Td 対称点群を持つアダマンタンに似ています。これは、同名の亜リン酸無水物であるP4O6と密接に関連しています。後者には末端オキソ基はありません。重さは 2.30 g/cm3、密度は 2.30 g/cm3 です。大気圧では 423°C で沸騰し、急速に加熱すると昇華する可能性があります。この形態は、五酸化リンの蒸気が急速に凝縮することによって生成され、吸湿性の高い固体が生成されます。
他の多形体は高分子ですが、それぞれ酸素原子の四面体を含み、そのうちの 1 つが末端を形成します末端酸素 p 軌道電子を反結合性リン-酸素単結合に供与することによる P=O リンク。高分子形態は、化合物を密閉チューブ内で数時間加熱し、溶融物を冷却して固体にする前に溶融物を高温に保つことによって生成できます。準安定な斜方晶「O」型 (密度 2.72 g/cm3、融点 562 °C) は、特定のポリシリケートと同様の多層構造を持ち、P6O6 環が相互に結合しています。安定した型は、O として知られる高密度の斜方晶相です。 ' 形。密度 3.5 g/cm3 の立体的なフレームワークで構成されています。最後の多形はガラス状または非晶質の物質で、他の物質を融合させることで作成できます。

準備:
四リン p4 が十分な酸素の存在下で燃焼すると、五酸化リンが生成されます。以下は化学反応です:
P4 + 5O2 =P4O10
この材料は純粋なリン酸源です.
ルイス構造:
P2O5 のルイス構造には、リンと酸素の 2 つの要素があります。五酸化リンのルイス構造では、2 つのリン原子が酸素原子 (P2O5) によって結合されています。 1 つおきの酸素原子が、リン原子と二重結合を形成しています。
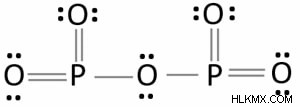
このルイス構造では、中心の酸素原子が 2 つのリン原子と単結合を形成しています。 3 つの酸素原子が各リン原子と結合しています。この分子には、4 つの (P=O) 二重結合が含まれています。 P2O5 のルイス構造では、原子に電荷はありません。
物理的特性
五酸化リンは無臭の白い粉です。
とても美味しく、水分を吸収しやすいです。
P4O10は化学式です。それにもかかわらず、それはその経験式 P2O5 から命名されています。
不燃性ですが、熱にさらされると爆発的に分解します。
五酸化リンのモル質量は 283.9 g/mol です。
2.39 g/cm3 は密度です。
この P2O5 の融点は 613K です。
沸点は華氏 633 度です。
化学的性質:
水と結合するとリン酸を生成する酸性化学物質です。
結晶化すると、4 つの異なる多形または形態で見つかります。
五酸化リンと水との間のプロセスである加水分解は、大量の熱を生成します。これは発熱プロセスです。
P4O10 + 6H2O → 4H3PO4 (–177 kJ )
アミドと反応するとニトリルに変換します。
P4O10 + RC(O)NH2 → P4O9(OH)2 + RCN
五酸化リンは非常に腐食性が高いため、金属から遠ざけてください。
アプリケーション:
水分を吸収する能力があるため、脱水剤として利用されます。このプロセスでは発熱が大きくなります。
P4O10 + 6 H2O → 4H3PO4 (–177 kJ).
粒状の P4O10 はデシケーターに使用されます。
また、いくつかの化学合成手順で第一級アミドからニトリルを作るためにも使用されます.
P4O10 + RC(O)NH2 → P4O9(OH)2 + RCN
リン化合物の製造に利用されています。
アルコールの酸化には、P4O10溶液である「小野寺試薬」が使われます。
光学ガラスや断熱ガラスの製造に利用されています。
乾燥剤としての使用は、広範囲の物質、特にそれが反応しない物質に利益をもたらします.
医薬品にはそれが含まれています。
農業では作物の肥料として使用されます。
五酸化リンが P4O10 と呼ばれるのはなぜですか?
P4O10 は五酸化リンとして知られています。理由.五酸化リンに関しては、式P2O5を持つ分子が結合して、P4O10のより大きな分子を生成します.そのため、五酸化リンの化学式は P4O10 ですが、その実験式 P2O5 から五酸化リンと呼ばれています。
結論:
水溶性が高く、発熱反応があります。アセトン、酢酸、ベンゼン、クロロホルムはすべて化合物に不溶です。爆発的な分解と発熱による加水分解は、2 つの重要な特徴です。それは主に脱水剤および乾燥剤として利用されています.五酸化リンはそれ自体では可燃性ではありません.このような相互作用の非常に発熱的な性質により、水や木や綿などの水を含むものと急速に反応し、多くの熱を放出し、おそらく火災を引き起こします.腐食性と刺激性が高く、わずかな濃度でも目、皮膚、粘膜、気道に深刻なやけどを引き起こします
1 mg/m3.