共有結合
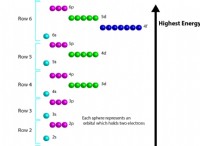
* 層: 共有結合は、2つ以上の原子が共有すると形成されます 安定した電子構成を実現する電子(通常は完全な外側シェル)。
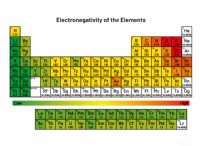
* 原子の種類: 通常、共有結合は非金属間で発生します。
* 結果: 分子が形成されます。これは、共有結合によって一緒に保持されている2つ以上の原子の中性グループです。
イオン結合
* 層: イオン結合は、1つの原子透過の場合に形成されます 別の原子から別の原子への電子。これにより、反対に帯電した2つのイオン(正と陰性)が作成されます。
* 原子の種類: イオン結合は通常、金属と非金属の間で発生します。
* 結果: イオン化合物が形成され、これは反対に帯電したイオン間の静電引力によって一緒に保持されます。
重要な違い: 主な違いは、共有結合が共有を含むことです 電子、イオン結合には移動が含まれます 電子。
例:
* 共有結合: 水(h 2 o)は、水素と酸素原子が電子を共有して共有結合を形成する分子です。
* イオン: テーブルソルト(NaCl)は、ナトリウム(Na)が電子を失い、Na + になるイオン化合物です。 、および塩素(Cl)が電子を獲得してCl - 。その後、反対に帯電したイオンは互いに引き付けられ、化合物を形成します。