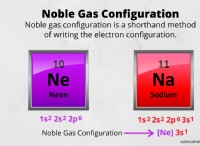
* 単一の共有結合: このタイプの絆には、 1つのペアの共有 2つの原子間の電子の。結合された原子のシンボル間の単一の線( - )で表されます。
* 例: メタン分子(CH4)では、各水素原子は炭素原子と1つの電子を共有し、4つの単一共有結合を形成します。
* 二重共有結合: このタイプの結合には、 2つのペアの共有 2つの原子間の電子の。結合された原子のシンボル間の二重線(=)で表されます。
* 例: エチレン分子(C2H4)では、2つの炭素原子が2組の電子を共有し、二重共有結合を形成します。
これが重要な違いを要約するテーブルです。
|機能|単一共有結合|二重共有結合|
| ------------------ | ------------------------- | --------------------------------------------------------------------------------------------
|電子ペア| 1つのペア| 2つのペア|
|表現|シングルライン( - )|ダブルライン(=)|
|結合強度|弱い|強い|
|結合長|長い|短い|
ここに簡単なアナロジーがあります:
手をつないでいる2人を考えてください。それは単一の絆です - 彼らは接続の1つのポイントを共有しています。今、彼らはまた他の手で手を握っていると想像してください。それは二重の絆です - 彼らは2つの接続ポイントを共有しています。
追加ポイント:
* 複数の結合: トリプル共有結合もあります(3組の電子を共有し、トリプルライン(いたずら)、さらには4倍結合さえありますが、これらはあまり一般的ではありません。
* 結合強度と長さ: 二重結合は、一般に、共有電子の2つのペアが原子間に強い魅力を生み出すため、単一結合よりも強く、短いです。
さらに説明したい場合はお知らせください!