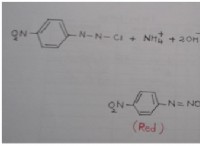
ブロンステッドローリー酸は、化学反応でプロトン(H+)を寄付する物質です。
この定義は、水素イオンが正に帯電している陽子の伝達に焦点を当てています。 ここにいくつかの重要なポイントがあります:
* プロトンドナー: 酸はプロトン(H+)を溶液に放出します。
* コンジュゲートベース: 酸がプロトンを寄付すると、その共役ベースを形成します。
* 平衡: 陽子の寄付と受け入れは可逆的である可能性があり、その結果、酸とその共役ベースの間に平衡が生じます。
例:
塩酸(HCl)と水との反応:
hcl +h₂o
* HClは、陽子(H+)を水に寄付するため、酸です。
* Cl-はHClの共役ベースです。
*H₃O+は、プロトンを受け入れる水分子によって形成された水素イオンです。
注:
ブロンステッド低下の定義は、酸のアレニウスの定義よりも広く、溶液中に水素イオン(H+)を生成する物質のみを考慮しています。