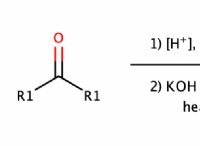
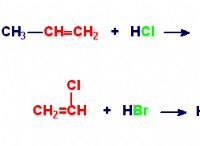
cr₂o₇²⁻(aq) +2oh⁻(aq)⇌2cro₄²⁻(aq) +h₂o(l)
これが反応の内訳です:
* 二クロム酸イオン(cr₂o₇²⁻): これらはオレンジ色の色です。
* 水酸化ナトリウム(NAOH): これは、水酸化物イオン(OH⁻)を提供する強力なベースです。
* クロム酸イオン(cro₄²⁻): これらは黄色です。
* 水(h₂o): 反応の副産物。
反応は可逆的であるため、両方向に進むことができます:
* 前方反応: 水酸化物イオン(OH⁻)を添加すると、二クロム酸イオン(cr₂o₇²⁻)を含む溶液に加えることで、クロム酸イオン(クロア²⁻)の形成が促進されます。溶液はオレンジの赤から黄色に変わります。
* 逆反応: クロム酸イオン(cro₄²⁻)を含む溶液に酸(h⁺)を追加すると、二染色酸イオン(cr₂o₇²⁻)の形成が促進されます。溶液は黄色からオレンジ色に変わります。
キーポイント:
*反応はpHの影響を受けます。 酸性溶液では、二クロマイトイオンが好まれていますが、基本的な溶液ではクロム酸イオンが好まれます。
*反応は平衡反応であり、反応物と産物の両方が溶液に存在することを意味します。
*この反応は、分析化学でよく使用されて、クロム酸イオンまたは二クロム酸イオンの濃度を決定します。
他に質問がある場合はお知らせください!