これが故障です:
* 価電子: これらは、原子の最も外側の殻の電子です。彼らは化学的結合に関与しています。
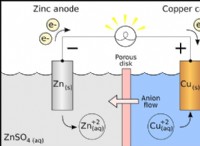
* 電子の伝達: 原子が1つ以上の価電子を失うと、それは正に帯電し、 cation と呼ばれます 。原子が1つ以上の価電子を獲得すると、それは負に帯電し、アニオンと呼ばれます 。
* イオン結合: 反対に帯電したイオン間の静電引力は、イオン結合を形成します 。
例:
ナトリウム(Na)には1つの価電子があり、塩素(Cl)には7つあります。ナトリウムがその価電子を失うと、それは正に帯電したナトリウムイオン(Na+)になります。塩素は電子を獲得し、負に帯電した塩化物イオン(Cl-)になります。 Na+とCl-の間の誘引は、一般にテーブル塩として知られているイオン化合物ナトリウム(NaCl)を形成します。