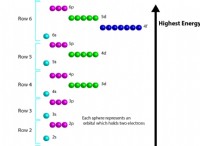
1。電子構成:
*両方に6つの原子価電子(最も外側のシェルの電子)があり、安定したオクテットを実現するために2つの電子を獲得する同様の傾向を与えます。
2。化学的特性:
* 非金属: 酸素と硫黄はどちらも非金属です。
* 酸化状態: どちらも負の酸化状態を示し(-2が最も一般的です)、酸化物と硫化物を形成できます。
* 酸の形成: どちらも水素と反応して酸(水(H₂O)と硫化水素(H₂S))を形成します。
3。物理的特性:
*両方とも、自然界では珪藻分子(o₂およびs₈)として見られます。
*両方とも人生に不可欠です。
違い:
* 電気陰性度: 酸素は硫黄よりも電気陰性です。つまり、電子をより強く引き付けます。これは、反応性の違いにつながります。
* 原子サイズ: 硫黄には、酸素よりも大きな原子半径があります。
* 室温での状態: 酸素は室温でのガスであり、硫黄は固体です。
要約すると、酸素と硫黄は周期表の位置のために多くの類似点を共有していますが、それらの異なる電気陰性度と原子サイズは化学的および物理的特性に明確な違いにつながります。