* 電気陰性度: 電気陰性度とは、原子が結合中に電子を引き付ける能力です。臭素(BR)は、ホウ素(B)よりも電気陰性です。 2つの要素間の電気陰性度の違いは、極性共有結合を作成するのに十分なほど重要です。
* イオン結合: イオン結合は、電子の完全な移動につながり、イオンを形成する電気陰性度(通常は1.7を超える)に大きな違いがある場合に発生します。これは、ホウ素と臭素の間では起こりません。
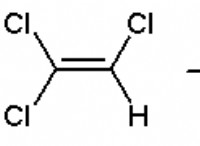
* 極性共有結合: 極性共有結合では、電子は不均等に共有されます。より電気陰性の原子が共有電子をより近づけ、その原子に部分的な負電荷(Δ-)を作成し、より少ない電気陰性原子に部分的な正電荷(Δ+)を作成します。
例: トリブロマイドホウ素(BBR3)の場合、臭素原子は共有電子を自分に向けて引っ張り、臭素原子をわずかに陰性にし、ホウ素原子をわずかに陽性にします。