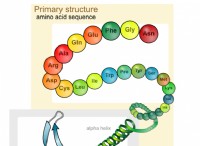
* 共有結合: これらには、原子間の電子の共有が含まれます。原子は、外側の電子シェルを満たす方法で電子を共有し、より安定させます。共有結合は強く、ほとんどの分子のバックボーンを形成します。
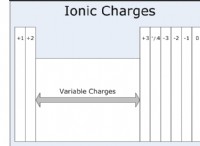
* イオン結合: これらには、ある原子から別の原子への電子の伝達が含まれます。 1つの原子は電子を失い、積極的に帯電します(陽イオン)、もう1つは電子を獲得し、負に帯電します(陰イオン)。反対の電荷が互いに引き付けられ、イオン結合が形成されます。
これら2つの主要なタイプに加えて、次のような分子の安定性に寄与する他のタイプの相互作用もあります。
* 水素結合: これらは、高強性原子(酸素や窒素など)と別の電気陰性原子に共有結合した水素原子との間に発生する弱い相互作用です。
* van der Waals Force: これらは、分子内の電子分布の一時的な変動から生じる弱い魅力です。
分子で原子を一緒に保持する結合の特定のタイプまたは結合の組み合わせは、関連する特定の原子とその電子構成に依存します。