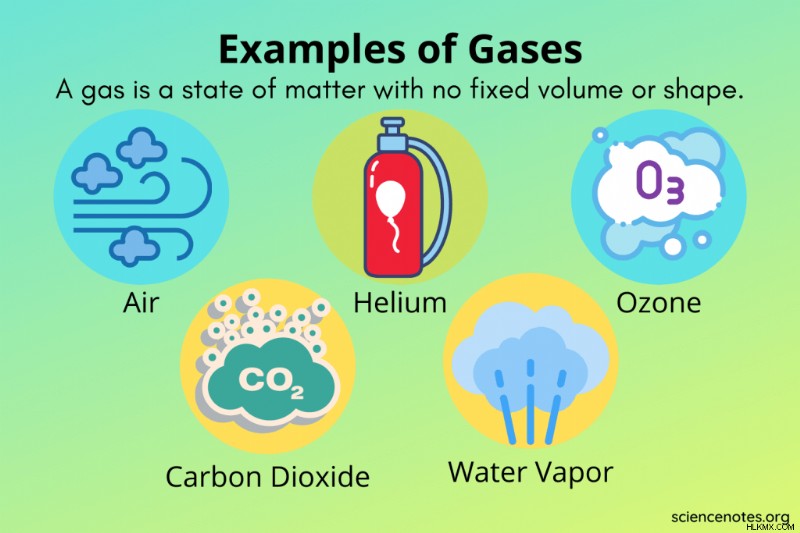
ガス 一定の体積や形を持たない物質の状態。言い換えれば、気体は容器の形と体積をとります。気体は凝縮して液体になるか、電離してプラズマになります。気体中の粒子は、液体中よりも互いに離れています。ガス粒子は、元素または化合物である可能性があります。気体は、純粋な物質 (例:酸素、ヘリウム、二酸化炭素) または混合物 (例:空気、天然ガス) のいずれかです。
ガスの例
以下はガスの例です:
- アセチレン
- 空気
- アルゴン
- 二酸化炭素
- 一酸化炭素
- ヘリウム
- 天然ガス
- ネオン
- 窒素
- 酸素
- オゾン
- プロパン
- 水蒸気
室温で気体である元素
いくつかの要素は、室温および常圧で気体です。水素、窒素、酸素、フッ素、および塩素は、等核二原子ガスを形成します。酸素はまた、等核三原子ガス、オゾンを形成します。オガネソンを除いて、すべての希ガス (ヘリウム、ネオン、アルゴン、クリプトン、キセノン、ラドン) は単原子ガスです。オガネソン (元素 118) は希ガス グループに属しますが、室温で固体である可能性があります。
- 水素 (H2)
- ヘリウム (He)
- 窒素 (N2)
- 酸素 (O2)
- オゾン (O3)
- フッ素 (Fl2)
- ネオン (Ne)
- 塩素 (Br2)
- アルゴン (Ar)
- クリプトン (Kr)
- キセノン (Xe)
- ラドン (Rn)
ガスと蒸気
「蒸気」という用語は、気体を表すために使用されることがあります。通常、蒸気とは、通常は別の状態にある物質の気体の形を指します。たとえば、水は通常、室温および圧力で液体です。その気体は水蒸気と呼ばれます。
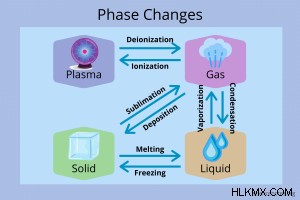
ガスが関与する相変化
気体は、プラズマ、液体、気体に変化します。さまざまな移行について学びます。
理想気体と実在気体の違い
化学と物理学は、理想気体と実在気体を区別します。理想気体は、気体の運動分子理論に従って振る舞い、理想気体の法則に従って振る舞います。基本的に、これは理想気体の粒子が体積をとらず、互いに引き付けられず、完全に弾性的な衝突で相互作用することを意味します。理想的な実在気体はありませんが、通常の温度と圧力の下では、それらの挙動は理想気体の法則を使用して近似することができるほど理想に近いものです。ただし、低温または高圧では、実在気体は理想的な挙動から大きく外れます。これは、高圧がガス分子をまとめ、それらの粒子サイズが重要になるためです。低温では、粒子は理想的に振る舞うのに十分な運動エネルギーを欠いています。それらは互いに引力を経験し、完全に弾性的な衝突で互いに跳ね返ることはありません。
参考文献
- Haynes, W. M., ed. (2016)。 化学および物理学の CRC ハンドブック (第96版)。フロリダ州ボカラトン:CRC Press/Taylor and Francis. ISBN 978-1482260960。
- ジョン、ジェームズ (1984)。 ガス力学 .アリンとベーコン。 ISBN 978-0-205-08014-4.