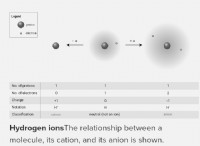
彼の実験が彼をこの結論に導いた方法は次のとおりです。
* カソード線実験: トムソンは、カソード光線が電界と磁場の両方によって偏向されることを観察しました。 これは、これらの光線が電荷を帯びていることを示し、その偏向パターンは、それらが負に帯電していることを示しました。彼は、これらの粒子の質量対電荷比を計算し、水素イオンの質量対電荷比よりもはるかに小さいことがわかりました。これは、彼が「電子」と呼ぶこれらの粒子が、最も小さな既知の原子よりもはるかに軽いことを示唆しています。
* 中性原子: 原子は電気的に中性であるため、トムソンは、電子の負電荷のバランスをとるために、原子に存在する積極的に帯電した材料が存在しなければならないと推論しました。
ただし、プラムプディングモデルは後に誤っていることが証明されました 1911年のラザフォードのゴールドフォイル実験により。この実験は、原子の質量の大部分が、電子が周囲に周囲を周回する一方で、小さな積極的に帯電した核に集中していることを示しました。
したがって、トムソンの原子に対する最初の理解は、電子が埋め込まれた均一で正に帯電した球の概念に基づいていました。 彼は積極的に帯電した粒子の存在を明示的に証明しませんでしたが、彼の研究は、後に原子核の発見への道を開いたモデルの発達につながりました。