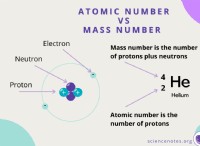
* 原子番号: 要素の特徴は、原子数であり、原子核内の陽子の数を表します。各要素には一意の原子番号があります。たとえば、すべての炭素原子には6つのプロトンがあり、すべての酸素原子には8つのプロトンがあります。
* 電子の数: 要素の原子は通常、プロトンと同じ数の電子を持ち、電気的に中性にします。この数の電子は、原子の化学的挙動にも影響します。
* 中性子の数: プロトンの数は元素を決定しますが、中性子の数は元素内で異なります。これらのバリエーションはアイソトープと呼ばれます。たとえば、炭素12には6つの中性子があり、炭素-14には8つの中性子があります。同じ元素の同位体は同様に化学的に動作しますが、質量は異なります。
* 電子構成: 核の周りの異なるエネルギーレベルと軌道における電子の配置は、各要素に固有です。この構成は、原子が他の原子とどのように相互作用するかに影響を与え、その化学的特性を決定します。
要約: 異なる元素の原子には異なる数のプロトンがあり、異なる電子構成と化学的挙動につながります。この根本的な違いは、それらを互いに区別します。