主な反応:
水溶液では、主要な反応は、ヨウ化カリウム(KI)とヨード酸カリウム(kio₃)の形成です。
3i₂ + 6 koh→5 ki +kio₃ + 3h₂o
説明:
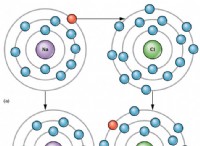
1。酸化還元: ヨウ素(I₂)は、酸化と還元の両方を受けます。
* 酸化: 一部のヨウ素はヨウ化するように酸化されています(io₃⁻)。
* 削減: 一部のヨウ素はヨウ化物(i⁻)に還元されます。
2。不釣り: この反応は、単一の要素が酸化と還元の両方を受ける不均衡の例です。
3。ベースアシスト: 水酸化カリウムは塩基として作用し、反応に必要な水酸化物イオン(OH⁻)を提供します。
その他の考慮事項:
* 温度: 反応は、より高い温度でより容易に進行します。
* 濃度: 反応物の濃度を増やすと、反応を加速できます。
* 他の酸化剤の存在: 他の酸化剤が存在する場合、反応はカリウム周期(kio₄)などの異なる製品を生成する可能性があります。
重要な注意:
*ヨウ素は水に控えめに溶けやすいため、反応は通常溶液中に行われます。
*反応は発熱性であり、熱を放出します。
追加の詳細:
この反応は、ヨウ化塩の一般的な成分であるヨウ化カリウムの生産に使用されます。副産物として生成されたヨウ酸カリウムは、他のヨウ素化合物を生成するためにさらに反応することができます。
他に質問がある場合はお知らせください!