* ナトリウム(Na) は金属であり、安定した電子構成を実現するために1つの電子を失う傾向があります。
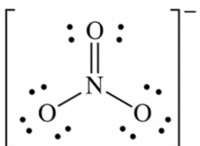
* 酸素(O) 非金属であり、安定した電子構成を実現するために2つの電子を獲得する傾向があります。
ナトリウムと酸素が反応すると、ナトリウム原子はそれぞれ1つの電子を失い、積極的に帯電したナトリウムイオン(Na⁺)を形成します。酸素原子は2つの電子を獲得し、負に帯電した酸化物イオン(O²⁻)を形成します。反対の電荷は互いに強く惹かれ、イオン結合として知られる静電魅力を形成します。
得られた化合物であるNa₂oは、正に帯電したナトリウムイオンと負に帯電した酸化物イオンとの間のこの静電的な力によってまとめられています。