これが故障です:
* 酸: 溶液中に水素イオン(H+)を寄付する物質。
* ベース: 溶液中の水素イオン(H+)を受け入れる物質。
* 塩: 塩基からの陽イオンが酸からの陰イオンと結合するときに形成されたイオン化合物。
* 水: 酸からの水素イオン(H+)と塩基からの水酸化物イオン(OH-)の反応から形成されました。
例:
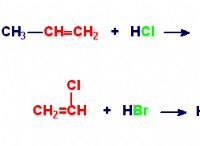
* 塩酸(HCl) +水酸化ナトリウム(NAOH)→塩化ナトリウム(NaCl) +水(H2O)
この反応は、塩(NaCl)と水(H2O)を生成する強酸(HCl)と強力な塩基(NaOH)の古典的な中和を示しています。