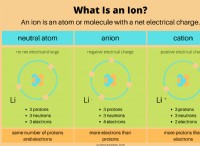
* カリウム(k) 高度に反応的なアルカリ金属です 。最も外側の電子を失う傾向が強く、積極的に帯電したイオン(K+)になります。
* 臭素(BR) ハロゲンです 非常に感動的です。これは、電子を獲得する強い傾向があり、負に帯電したイオン(BR-)になることを意味します。
カリウムと臭素が接触すると、彼らは激しく反応して臭化カリウム(KBR):
2k(s) + br2(l)→2kbr(s)
これがこの反応が起こる理由です:
1。静電引力: 陽性に帯電したカリウムイオン(K+)および負に帯電した臭化物イオン(BR-)は、静電力のために互いに強く引き付けられます。
2。エネルギー放出: カリウムと臭素の間のイオン結合の形成は、かなりの量のエネルギーを放出し、反応を発熱します(熱放出)。
3。安定性: 臭化カリウムの形成は、カリウムと臭素の両方の原子の両方でより安定した構成をもたらし、その電子構成を満たし、より低いエネルギー状態を達成します。
重要な注意: この反応は非常に発熱性であり、多くの熱を生成します。潜在的な危険のため、制御された環境で訓練された専門家がのみ実行する必要があります。