その理由は次のとおりです。
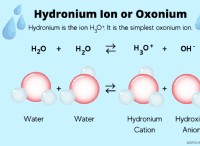
* 弱酸は水中で完全にイオン化しないでください。 それらは、水素イオン(H+)を部分的にしか寄付しません。つまり、強酸と比較して溶液中のH+イオンの濃度が低いことを意味します。
* pHは、H+イオンの濃度の尺度です。 H+イオンの濃度が低いと、pH値が高くなります。
キーポイント:
* 弱酸の正確なpHは、その特定の解離定数(ka)に依存します。 KA値が高いほど、酸が強いことを示します(より多くのイオン化)。
* 弱酸のpHはその濃度にも依存します。 より濃縮された弱酸は、より低いpH(より多くのH+イオン)を持ちます。
例:
酢酸(CH3COOH)は弱酸です。 0.1 mの酢酸溶液のpHは3よりわずかに少なくなり、0.1 M溶液の塩酸(HCl、強酸)のpHは1のpHです。
要約:
弱酸にはpHがあります。
* 7(酸性)未満
* 同じ濃度での強酸のpHより大きい
* 酸の解離定数(ka)とその濃度によって決定されます。