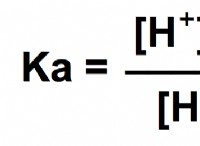1。モルリティを理解する
Molality(M)は、溶媒1キログラムあたりの溶質のモルとして定義される濃度の尺度です。
2。溶質と溶媒を識別します
* 溶質: Chromium(CR)は、より少ない量で存在するコンポーネントです。
* 溶媒: 鉄(Fe)は、大量に存在するコンポーネントです。
3。質量をモルに変換します
* クロム:
-Crのモル質量=51.996 g/mol
-cr =(0.125 g) /(51.996 g / mol)=0.00240 molのモル
4。溶媒の質量をキログラムに変換します
* 鉄:
- fe =81.3 gの質量
-kg =(81.3 g) /(1000 g / kg)=0.0813 kgのFeの質量
5。 Molality を計算します
* Molality(M)=(溶質のモル) /(溶媒のキログラム)
* Molality(M)=(0.00240 mol)/(0.0813 kg)= 0.0295 mol/kg
したがって、固溶体のモルリアルは約0.0295 mol/kgです。