* アンモニウムイオン(nh₄⁺): アンモニウムイオンは、弱い塩基であるアンモニア(nh₃)のコンジュゲート酸です。アンモニウムイオンが水中にある場合、プロトン(H⁺)を寄付することができ、溶液をより酸性にします。
* 硫酸イオン(so₄²⁻): 硫酸イオンは、強酸(硫酸、h₂SO₄)の共役塩基です。溶液のpHに大きく影響しません。
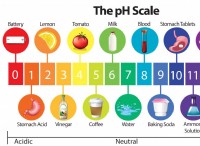
したがって、硫酸アンモニウム溶液のpHは7未満で、酸性になります。
正確なpH値は、硫酸アンモニウム溶液の濃度に依存します。
重要な注意: 硫酸アンモニウム溶液のpHは、温度や他のイオンの存在などの要因によって異なります。