あなたが説明している反応は、実際にはアンモニア(nh₃)の間です および塩化水素(HCl) 塩化アンモニウム(nh₄cl)を生成する 。
これがバランスの取れた化学式です:
nh₃(g) + hcl(g)→nh₄cl(s)
これはガス相反応です アンモニアと塩化水素ガスが反応して、塩化する固体アンモニウムを形成します。
これが何が起こるかの内訳です:
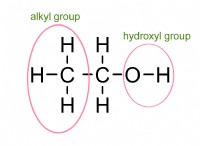
* アンモニア(nh₃): アンモニアは弱い塩基です。つまり、陽子(H⁺)を受け入れることができます。
* 塩化水素(HCl): 塩化水素は強酸です。つまり、プロトン(H⁺)を容易に寄付します。
* 反応: アンモニアの窒素原子の電子の孤独なペアは、塩化水素からプロトンを引き付けます。これにより、窒素と水素の間に新しい結合が形成され、アンモニウムイオン(NH₄⁺)が生成されます。残りの塩化物イオン(Cl⁻)は、アンモニウムイオンと結合して塩化アンモニウムを形成します。
この反応は、中和反応の例です 、酸と塩基が反応して塩(塩化アンモニウム)と水を形成します。ただし、この場合、反応が気相で発生するため、水は生成されません。
反応は非常に発熱です 、進行するにつれて熱を放出します。これが、アンモニアと塩化水素ガスが混合されているときに白い煙が形成されるのをよく見る理由です。この煙は、実際には反応によって形成された固体塩化アンモニウム粒子です。