1。溶質を追加
*最も簡単な方法は、溶液(溶質)を溶液にさらに追加することです。
*例:砂糖を1杯の水に追加すると、砂糖溶液がより濃縮されます。
2。溶媒を取り外します
*溶媒(溶解を行う物質)の一部を除去することにより、溶液をより濃縮することもできます。
*例:塩水溶液を蒸発させると、水が蒸発し、より濃縮された塩溶液が残ります。
3。より可溶性溶質を使用します
*固体溶質を使用している場合、より溶けやすい形の物質を使用して濃度を増やすことがあります。
*例:砂糖は、同様の砂の塊よりも速く、より高い濃度に溶解します。
重要な考慮事項:
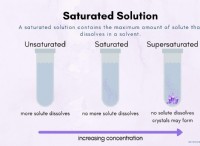
* 溶解度制限: 特定の温度で特定の溶媒に溶解できる溶質の量には制限があることに注意してください。これは溶解度と呼ばれます 溶質の。 溶解度の制限に到達すると、溶質を追加すると、容器の底部に溶解していない固体が生じます。
* 飽和: 特定の温度で可能な溶質の最大量を含む溶液は、a 飽和溶液と呼ばれます 。 飽和溶液に溶質を追加しても、濃度は増加しません。
* 過飽和: 特定の条件下では、通常可能なよりも多くの溶質を含む超飽和ソリューションを作成することがあります。 ただし、これらの溶液は不安定であり、過剰な溶質は最終的に溶液から結晶化します。
特定のシナリオを念頭に置いている場合はお知らせください。もっとテーラードアドバイスを提供できます!