複合イオンの形成:
* 塩化アルミニウム(ALCL3) ルイス酸です。つまり、電子ペアを受け入れることができます。
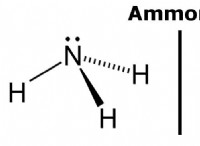
* アンモニア(NH3) ルイスベースであり、電子ペアを寄付できることを意味します。
これら2つが反応すると、アンモニア分子は孤立した電子ペアをアルミニウムイオンに寄付し、複合イオンを形成します。形成される最も一般的な複合体は、テトラミニアルミニウム(III)イオン[al(nh3)4]³⁺です 。
反応化学量論:
反応は次のように表現できます。
alcl3 + 4 NH3→[al(nh3)4]³⁺ + 3cl⁻
この方程式は、1モルのALCL3が4モルのNH3と反応することを示しています。これは 1:4モル比です 、1:1ではありません。
比率に影響する要因:
* 濃度: より高いアンモニア濃度は、より複雑なイオンの形成を支持します。
* 温度: 温度の上昇は、平衡を反応物に向かってシフトする可能性があります。
* 溶媒: 使用される溶媒は、複合イオンの安定性に影響を与える可能性があります。
結論:
塩化アルミニウムとアンモニアの反応は複雑であり、単純な1:1の比率には従いません。比率は通常1:4で、テトラミニアルミニウム(III)複合体イオンを形成します。ただし、特定の比率は反応条件によって異なります。