アルカリ土類金属またはアルカリ土類は、周期表の 2 番目のグループ (列) にある 6 つの元素のセットです。これらの各元素の原子は、外側の電子殻に 2 つの電子を持っています。このグループの要素とその共通のプロパティを見てみましょう:
アルカリ土類金属のリスト
6つのアルカリ土類があります。原子番号の昇順に並べると、次のようになります:
- ベリリウム (Be)
- マグネシウム (Mg)
- カルシウム (Ca)
- ストロンチウム (Sr)
- ラジウム (Ra)
- 元素 120 は、発見されるとアルカリ土類になります。
アルカリ土類金属の特性

各原子には 2 つの価電子があるため、このグループの元素にはいくつかの共通の特徴があります:
- アトムには完全な外側 があります 電子殻 (2 個の電子)。これは、これらの元素が 2+ の電荷を持つ陽イオンを形成し、2+ の酸化状態を持つことを意味します。
- 原子は電子親和力が低く、電気陰性度が低い
- アルカリ土類はすべて、常温常圧で光沢のある銀色の金属です。
- これらの金属は可鍛性と延性があります。
- アルカリ土類金属は柔らかく、金属の密度、融点、沸点が比較的低い傾向があります。融点と沸点は、非金属よりもはるかに高いです。これらの元素は柔らかいですが、アルカリ金属グループの元素よりも硬いです。
- このグループの元素は適度に反応性が高く、周期表の下に行くにつれて反応性が高くなります (つまり、ストロンチウムはカルシウムよりも反応性が高い)。
- アルカリ土類金属は化合物に含まれており、遊離しているものではありません。
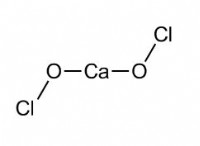
- アルカリ土類は、ハロゲン (Cl、Br など) と容易に反応してハロゲン化物を形成します。また、酸素と反応して酸化物を形成します。
- それ自体は特性ではありませんが、すべてのアルカリ土類元素はその酸化物 (アルカリ土類) にちなんで命名されており、ベリリア、マグネシア、石灰、ストロンシア、バリタなどの名前が付けられていることに注意してください。