* 酸性度と塩基性: 酸性度と塩基性は、物質が陽子を寄付または受け入れる傾向によって決定されます(H⁺イオン)。
* 酸 陽子を寄付します。
* ベース プロトンを受け入れます。
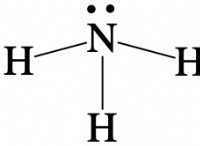
* アンモニアの構造: アンモニアには、窒素原子に孤立した電子のペアがあります。この孤独なペアは陽子を容易に受け入れ、アンモニアを塩基にします。
* 水の構造: 水には、酸素原子に孤立した電子もあります。ただし、酸素原子は窒素よりも電気陰性です。これは、電子をよりしっかりと保持し、プロトンを受け入れる可能性が低くなることを意味します。
* KB値: ベース解離定数(KB)は、ベースの強度の尺度です。 KB値が高いほど、ベースが強くなります。アンモニアのkbは1.8 x10μであり、水のKBは1.0 x 10°ofです。これは、アンモニアが水よりも強いベースであることを明確に示しています。
要約: アンモニアの窒素原子は、容易に利用可能な孤立した電子ペアを備えたもので、水よりも強い塩基になり、電子がよりしっかりと保持されます。