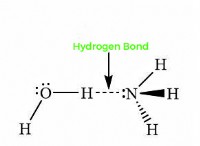
* 否定性は相対的です: 化学では、「否定性」は次のようなさまざまな概念を指すことができます。
* 電気陰性度: これは、結合中に電子を引き付ける原子の傾向を説明しています。
* チャージ: これは、分子またはイオンの全体的な電気バランスを説明しています。負電荷は、陽子よりも多くの電子があることを意味します。
* 化学変化は複雑です: 化学変化には、原子と分子の再配置が含まれます。 これらの再配置は電気陰性または電荷を変える可能性がありますが、「否定性」の単純な増加または減少ではありません。
「よりネガティブ」の代わりに、化学変化を説明する正確な方法をいくつか紹介します:
* 削減: これには、酸化状態の減少(電子損失またはゲインの尺度)の減少につながる可能性のある電子の獲得が含まれます。
* 電子のゲイン: これにより、種の負の電荷が直接増加します。
* 陰イオンの形成: アニオンは、原子が電子を獲得するときに形成される負に帯電したイオンです。
例:
ナトリウム(Na)と塩素(Cl)との反応において、塩化ナトリウム(NaCl)を形成します。
* ナトリウム(Na)は電子を失います: これは酸化であり、ナトリウムは正の帯電イオン(Na+)になります。
* 塩素(Cl)は電子を獲得します: これは減少であり、塩素は負に帯電したイオン(CL-)になります。
キーテイクアウト: 「よりネガティブ」に焦点を合わせる代わりに、化学反応中の電気陰性度、電荷、または酸化状態の特定の変化を考慮してください。