イオン化合物
* 結合: 正の帯電イオン(陽イオン)と負に帯電したイオン(アニオン)の間の静電引力によって形成されます。これには、ある原子から別の原子への電子の完全な伝達が含まれます。
* 層: 通常、金属と非金属の間に形成されます。
* 構造: 通常、繰り返し3次元格子構造を持つ結晶性固体として存在します。
* プロパティ:
* 高融点と沸点: 強い静電力は、壊れるのにかなりのエネルギーを必要とします。
* 水に溶けたり溶けたりしたときに電気を伝導します: 自由イオンが存在し、電荷の流れが可能になります。
* しばしば脆い: 剛性構造は、ストレスによって簡単に破壊されます。
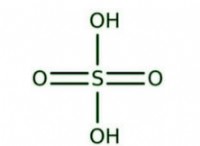
* 例: 塩化ナトリウム(NaCl)、酸化カルシウム(CAO)、硫酸マグネシウム(MGSO₄)
分子共有化合物
* 結合: 2つの非金属原子間の電子の共有によって形成されます。
* 層: 通常、非金属間に形成されます。
* 構造: 分子の形状に応じて、さまざまな形のガス、液体、または固体として存在することができます。
* プロパティ:
* 融点と沸点の低い: 分子間の分子間力が弱い場合、克服するエネルギーが少なくなります。
* 一般的に貧弱な電気導体: 遊離イオンは存在しません。
* 室温での固体、液体、またはガスにすることができます: 分子間力の強度に応じて。
* 例: 水(h₂o)、二酸化炭素(CO₂)、メタン(ch₄)
主要な違いを要約するテーブルです:
|機能|イオン化合物|分子共有化合物|
| ------------------ | -------------------------------- | ---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
|結合|イオン間の静電引力|電子の共有|
|フォーメーション|金属 +非金属|非金属 +非金属|
|構造|結晶固体|さまざまな(ガス、液体、固体)|
|融解/沸騰|高|低い|
|導電率|溶解/溶けたときは良い|貧しい|
覚えておいてください: 「イオン」および「共有」という用語は、化合物内の結合の種類を指します。全体の化合物は、存在する結合の種類に関係なく、依然として固体、液体、またはガスである可能性があります。