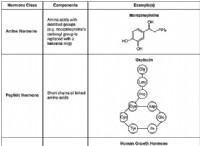
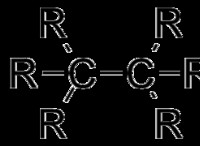
イオン結合
* 結合の性質: イオン結合には転送が含まれます ある原子から別の原子への電子の。
* 電気陰性度: 電気陰性度に大きな違いがある原子 (電子を引き付ける能力)イオン結合を形成します。通常、金属(電気陰性度が低い)は、電子を非金属(高い電気陰性度)に失います。
* 結果のイオン: 電子の伝達はイオンを作成します :
* カチオン: 電子の損失(金属)によって形成される正の帯電イオン。
* アニオン: 電子の獲得(非金属)によって形成される負の帯電イオン。
* 結合強度: イオン結合は一般により強いです 共有結合よりも。
* 化合物の特性: イオン化合物は通常、結晶を形成します 融点と沸点が高い。それらは、電気の良好な導体ですです 水に溶けたり溶けたとき。
* 例: 塩化ナトリウム(NaCl)、酸化マグネシウム(MGO)、フッ化物カルシウム(CAF₂)。
共有結合
* 結合の性質: 共有結合には共有が含まれます 2つの原子間の電子の。
* 電気陰性度: 同様の電気陰性度を持つ原子 共有結合を形成します。これは、原子が両方とも均等に電子を引き付けることができることを意味します。
* 結果の分子: 共有電子は分子で原子を一緒に保持します 。
* 結合強度: 共有結合は、共有電子の数と原子のサイズに応じて強度が異なる場合があります。 それらは一般的に弱いです イオン結合より。
* 化合物の特性: 共有化合物は、ガス、液体、または固形物であるになります 室温で。それらは、電気の導体が不十分です 。
* 例: 水(H₂O)、二酸化炭素(CO₂)、メタン(Ch₄)。
有用なアナロジー
イオン結合は と考えてください 誰か(電子)からの何かと共有結合共有 何か(電子)。
重要な注意: また、電子が電気陰性度の違いにより不均等に共有されるが、イオン結合ほど大きくない「極性共有結合」もあります。これにより、分子の原子に部分的な正および部分的な負電荷が生成されます。