1。結合および電子構成:
* so₂: 二酸化硫黄には、硫黄と各酸素原子の間に二重結合があります。硫黄原子は、3D軌道を利用して二重結合からの余分な電子を収容し、硫黄と酸素の両方に安定したオクテット構成をもたらします。
* so: 一酸化硫黄には、硫黄と酸素の間に単一の結合しかありません。これにより、硫黄原子に不完全なオクテットが残され、非常に反応性と不安定になります。
2。共鳴構造:
* so₂: 二酸化硫黄は共鳴を示します。つまり、その電子は分子全体で非局在化されています。この非局在化は、分子の安定性に貢献します。
* so: 一酸化硫黄には共鳴構造がなく、安定性が低下します。
3。熱力学的考慮事項:
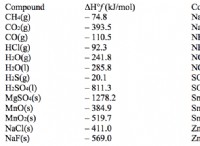
* so₂: 硫黄と酸素からのSO₂の形成は発熱性であり、エネルギーを放出し、安定した製品を示しています。
* so: 硫黄と酸素からのSOの形成は発熱性が低く、安定性が低いことを示唆しています。
4。酸化状態:
* so₂: SO₂では、硫黄の酸化状態は+4です。これは、SOの+2酸化状態と比較して、硫黄にとってより安定した酸化状態です。
5。分子形状:
* so₂: 二酸化硫黄は、より好ましい電子分布を提供し、エレクトロニクス間反発を減少させる曲がった分子形状を持っています。
* so: 一酸化硫黄は線形形状で、電子反発の可能性があるため安定性が低くなります。
要約:
二酸化硫黄の二重結合、共鳴、好ましい酸化状態、発熱形成、および曲がった分子形状は、一酸化硫黄と比較してより大きな安定性に寄与します。