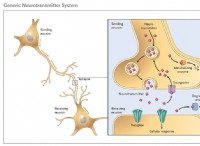
* 金属債の性質: 金属結合は、多くの金属原子間で非局在化した電子を共有することによって形成されます。これらの電子は、金属構造全体を通して自由に移動でき、金属は導電率や順応性などの特徴的な特性を与えます。
* 水の極性: 水は極性分子です。つまり、水素と酸素原子の間の電子の不均等な共有により、正の端と負の端があります。
* 魅力の欠如: 金属の非局在電子は、水分子の正または負の端に引き付けられません。水分子は主にイオンまたは極分子に引き付けられます。
したがって、水分子は金属原子を一緒に保持している強力な金属結合をバラバラにすることができません。
例外:
* 特定の金属イオン: 一部の金属イオン(ナトリウムイオンなど)は、水分子とイオン結合を形成するため、水に溶解する可能性があります。ただし、これは金属自体内の金属結合の破壊によるものではありません。
* 合金: 金属の混合物である一部の合金は、水と反応して酸化物または水酸化物を形成する可能性があります。ただし、これは化学反応であり、単純な溶解プロセスではありません。
要約: 水は金属結合を溶解しません。なぜなら、それはそれらを壊すために必要な魅力を欠いているからです。