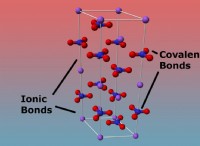
* 多原子イオン: これらは、共有結合して純電荷を運ぶ原子のグループです。それらは、イオン化合物の単一ユニットとして機能します。例は次のとおりです。
* 硝酸塩(no₃⁻): このイオンは窒素と酸素で構成されており、負電荷を負います。
* リン酸(po₄³⁻): このイオンはリンと酸素で構成されており、トリプルマイナス電荷を運びます。
* アンモニウム(nh₄⁺): このイオンは窒素と水素で構成されており、正電荷を持ちます。
* 複数のカチオンと陰イオン: イオン化合物は、複数のタイプの陽イオンと陰イオンの組み合わせによって形成されます。これらの化合物には、多くの場合、複雑な名前と式があります。例は次のとおりです。
* リン酸カルシウム(ca₃(po₄)₂): この化合物は、カルシウムイオン(ca²⁺)とリン酸イオン(po₄³⁻)を組み合わせて形成されます。
* 硫酸カリウム(kal(so₄)₂): この化合物は、カリウムイオン(k⁺)、アルミニウムイオン(al謝)、および硫酸イオン(so₄²⁻)を組み合わせて形成されます。
本質的に、イオン化合物の複雑さは、さまざまな元素と多原子イオンを組み合わせて、化合物の全体的な電気中立性を満たす可能性から生じます。この式は、この中立性を達成するために必要なイオンの最も単純な全数比を表しています。