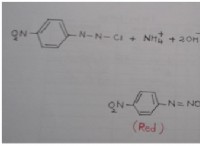
反応
一般的な反応は次のようになります:
* 酸 +金属炭酸塩→塩 +水 +二酸化炭素
例
一般的な例は、塩酸(HCl)と炭酸カルシウム(Caco₃)の反応です。
* 2 hcl(aq) +caco₃(s)→cacl₂(aq) +h₂o(l) +co₂(g)
説明
1。酸は水素イオンを提供します: 酸(HClなど)は、溶液中の水素イオン(H⁺)を放出します。
2。炭酸塩は炭酸塩イオンを提供します: 金属炭酸塩(CACO₃など)は、溶液中の炭酸イオン(Co₃²⁻)を放出します。
3。炭酸酸の形成: 酸からの水素イオンは、炭酸塩イオンと反応して炭酸酸(H₂Co₃)を形成します。
4。炭酸酸の分解: 炭酸酸は不安定で、すぐに水(H₂O)と二酸化炭素ガス(CO₂)に分解します。
反応を観察する
あなたは気づく:
* Fizzing/Bubbling: 二酸化炭素ガスの放出は、溶液中に泡立ったり泡立ったりします。
* ガス生産: 多くの場合、倒立容器に水を置換することにより、二酸化炭素ガスを収集できます。
* 塩形成: 溶液中の残りのイオン(この例のカルシウムおよび塩化物イオン)が組み合わせて、塩(塩化カルシウム)を形成します。
安全対策
*酸を扱うときは、常に安全ゴーグルを着用してください。
*換気の良いエリアで実験を実施します。
*酸との直接接触は避けてください。
さまざまな酸と金属炭酸塩を使用して、より具体的な反応の例を見たい場合はお知らせください!