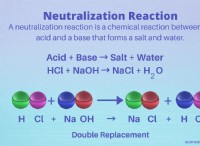
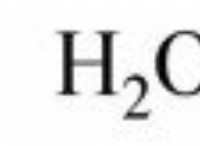* 共有結合: 水分子は共有結合によって形成されます 水素と酸素原子の間。共有結合では、原子は電子をイオン結合のように伝達するのではなく、電子を共有します。
* 極性: 水分子内の結合は共有結合ですが、分子自体は極性です 。これは、電子が酸素と水素原子の間で等しく共有されないことを意味します。酸素はより電気陰性であるため、電子をより強く引き付けることを意味します。これにより、分子の酸素側にわずかな負電荷が生じ、水素側にわずかな正電荷が生成されます。
* 水素結合: 水分子の極性により、水素結合を形成することができます お互いに。 水素結合は共有結合よりも弱いが、それでも水のユニークな特性に寄与している。
重要な注意: 純水は非イオン性ですが、イオン化合物を溶解できます 。これは、水分子の極性がイオンを引き付けて囲み、互いに効果的に分離できるためです。これが、水が多くの塩に適した溶媒である理由です。