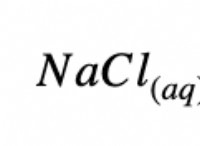これがそれが意味することです:
* 同位体 同じ数のプロトン(要素を定義する)があるのと同じ数の中性子を持つ同じ要素の原子です。中性子数のこの違いは、原子質量の変動につながります。
例:
* 炭素の同位体: 炭素-12(⁶¹²c)、炭素-13(⁶¹³c)、および炭素-14(⁶¹⁴c)はすべて炭素の同位体です。それらは同じ数の陽子(6)ですが、異なる数の中性子(それぞれ6、7、および8)があります。
* ウランの同位体: ウラン-235(⁹²³⁵U)およびウラン-238(⁹²³⁸U)は、核エネルギーおよび武器で使用されるウランの同位体です。
化学における「ISO」の他の使用:
* 異性体: 同じ化学式であるが、異なる構造配置を持つ分子。
* Isobaric: 同じ質量数(陽子と中性子の総数)を持つ原子または核を指す。
「ISO」は同位体に最も一般的に関連付けられていますが、特定の化学用語でその意味を理解するためにコンテキストを考慮することが重要です。