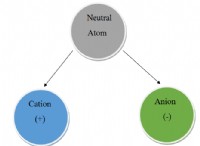
* 中性酸素原子: 酸素には8つのプロトンと8つの電子があり、中性電荷を与えます。その電子構成は1s 2 です 2S 2 2p 4 。
* 電子の獲得: 酸素の電気陰性度は高いため、電子を強く引き付けることを意味します。 安定したオクテット(最も外側のシェルに8電子)を実現するには、2つの電子を獲得する必要があります。
* 酸化物イオン形成: 酸素が2つの電子を獲得すると、酸化物イオンになります(O 2- )。その電子構成は現在、ノーブルガスネオンの構成に似ており、最も外側のシェルがあります(1s 2 2S 2 2p 6 )。
ここに単純な方程式があります:
o + 2e - →O 2-
例:
酸化マグネシウム(MGO)の形成では、マグネシウム(MG)は2つの電子を失い、Mg 2+ になります 、そして酸素がこれらの2つの電子を獲得してO 2- 。これらの反対に帯電したイオンは、互いに引き付けられ、イオン結合を形成します。
キーポイント:
*酸化物イオンは非常に反応性があり、通常はイオン化合物に存在します。
*彼らは、酸化反応、塩基の形成、多くの無機材料の作成など、さまざまな化学プロセスで重要な役割を果たします。