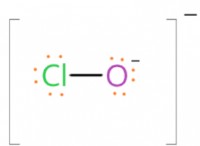* 電子構成: 塩素には17個の電子があります。その電子構成は2-8-7です。これは、最も外側のシェル(価数シェル)に7つの電子があることを意味します。
* オクテットルール: 原子は、最も外側のシェルに8つの電子がある場合、最も安定している傾向があります。これはOctetルールとして知られています。
* 電子の獲得: 塩素は、1つの電子を獲得することにより、安定したオクテットを達成できます。これにより、最も外側のシェルに合計8つの電子が得られ、構成は2-8-8になります。
* cl-:の形成 塩素が電子を獲得すると、それは負に帯電し、塩化物イオン(Cl-)を形成します。
本質的に、塩素は電子を獲得します。なぜなら、安定した構成を実現するために7つの電子を失うよりも、1つの電子を獲得するのが安定したオクテットに到達するのが簡単だからです。これが、塩素が非常に反応性があり、負のイオンを容易に形成する理由です。