酸素は、金属または非金属と反応すると、一般に酸化物を形成します。他の酸化物と同様に、酸素がハロゲンファミリーと反応する場合、それはオキシ酸またはオキシ酸用です。ハロゲンファミリーに加えて、ホウ素、窒素、硫黄、およびリンと酸素酸を形成することができます.ハロゲンのオキソ酸には、次亜ハロゲン酸(HOX)、亜ハロゲン酸(HOXO)、ハロゲン酸(HOXO2 )、および過ハロゲン酸 (HOXO3 )。このように、+1 の酸化状態を持つ塩素のオキソ酸は、次亜塩素酸 (HOCl) です。イオン形態では、次亜塩素酸 (ClO) イオンとして存在します。しかし、この次亜塩素酸イオンは、一塩基酸以外にもさまざまな主要な次亜塩素酸塩を形成できることをご存知ですか?この記事を見て、次亜塩素酸とイオン、およびそれらの用途と特性について詳しく知りましょう.
次亜塩素酸イオンとは?
次亜塩素酸塩は、ハロゲンのオキソ酸から形成される塩です。次亜塩素酸イオン、つまりClOイオンが含まれています。これらの次亜塩素酸イオンに特定の陽イオンが結合すると、異なる次亜塩素酸塩が形成されます。最も一般的な一塩基性次亜塩素酸の式は HClO で、次亜塩素酸としても知られています。
次亜塩素酸ナトリウム (NaClO)、次亜塩素酸カルシウム [Ca(ClO)2 ]、および次亜塩素酸カルシウム [CaCl(OCl)] または (CaOCl2 ) は、その他の重要な次亜塩素酸塩です。クロロ次亜塩素酸カルシウムは漂白剤としても知られています。同時に、次亜塩素酸ナトリウムの溶液は漂白液としても知られており、繊維産業で漂白目的で使用されています.
次亜塩素酸塩の歴史
1789 年、フランスのジャベルで次亜塩素酸塩が初めて生産されました。これは、炭酸ナトリウム溶液に塩素ガスを通すことによって生成されました。得られた液体は、Javelle水またはEau de Javelleとして知られる弱い次亜塩素酸ナトリウム溶液でした.しかし、それは効率的ではなかったため、化学者は他の製造方法を探しました。 19世紀、E.S。スミスは次亜塩素酸塩の製造方法を開発し、特許を取得しました。彼のプロセスによれば、塩水が加水分解されて塩素ガスと苛性ソーダが生成されます。その後、混合して次亜塩素酸塩を形成します。今日では、フッカー プロセスとして知られる、この方法の改良版が使用されています。このプロセスは、次亜塩素酸ナトリウムを生産する唯一の大規模な工業的方法です。
次亜塩素酸イオンの構造と形状
次亜塩素酸イオンは負電荷を 1 つ持っているため、負電荷を帯びた酸素原子が 1 つ含まれています。この O 原子は一価であり、単結合、すなわち (Cl-O) 𝜎 結合を介して Cl 原子と結合します。このイオンの電子ドット構造は、オクテット規則に従うことを示しており、その中で、Cl 原子は 1 つの 𝜎 結合によって O 原子と結合し、3 つの孤立電子対を持っています。したがって、Cl 原子は 1 つの 𝜎 結合と 3 つの孤立電子対に囲まれているため、この原子は sp3 混成です。 Cl 原子の混成軌道は、O イオンの混成軌道と重なり、(Cl-O) 𝜎 結合を形成します。 Cl 原子には 3 つの非共有電子対が存在するため、ClO イオンは四面体の形状ではなく、線形の形状をしています。 ClO- イオンの Cl-O 結合距離は 1.69Å に等しく、Cl-O 結合エネルギーは 209 kJ/mol です。
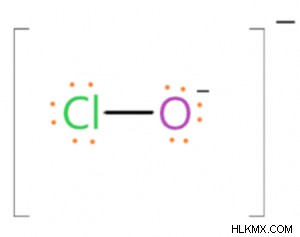
次亜塩素酸塩の製造
1.アルカリまたはアルカリ土類金属水酸化物との反応:
次亜塩素酸塩は、塩素をアルカリまたはアルカリ土類金属の水酸化物と反応させると生成されます。
Cl2 + 2NaOH → NaCl + NaClO + H2 O
2Cl2 + 2Ca(OH)2 → CaCl2 + Ca(ClO)2 + 2H2 O
これらの反応は、塩素酸塩の生成を抑えるために室温付近で行われます。
2.電気化学プロセスによる:
このプロセスでは、塩水が電気分解されて Cl2 が形成されます。 、水中で解離して次亜塩素酸塩を形成します。
2Cl → Cl2 + 2e
Cl2 + H2 O ⇌ HClO + Cl + H
3.金属硫酸塩との反応:
次亜塩素酸カルシウムが金属硫酸塩と反応すると、金属次亜塩素酸塩と硫酸カルシウムが生成されます。この反応は水中で行われます。
Ca(ClO)2 + MSO4 → M(ClO)2 + CaSO4
次亜塩素酸イオンの性質
その特性に基づいて、そのプロパティは次のように分類されます
1.物理的特性:
- 塩素のオキソ酸イオンの IUPAC 名は次亜塩素酸塩です。
- 次亜塩素酸の式は ClO です。
- 次亜塩素酸塩の分子量は 51.449 g/mol です。
- 固体で、40°C で分解します。
- 水に溶けます。
- 次亜塩素酸 (HClO) はその共役酸です。
- これは、塩素酸化物、塩素オキソアニオン、および 1 価の無機アニオンです。
- 摂取および吸入すると有毒です
2.化学的性質:
- 酸性化すると、次亜塩素酸塩は次亜塩素酸を生成します。この反応は、塩素ガスと平衡状態で存在します。
2H + ClO + Cl ⇌ Cl2 + H2 O
- 加熱すると、次亜塩素酸塩は塩化物、酸素、その他の塩素酸塩に分解されます。
2ClO → 2Cl + O2
3ClO → 2Cl + ClO3
- 非常に不安定で、溶液の形でしか存在できません。
- 次亜塩素酸カルシウムは安定性が高く、工業規模で生産されています。
- 純粋な次亜塩素酸マグネシウムは調製できません。
- 加熱時、LiOCl および Ca(OCl)2 危険な熱暴走を引き起こし、爆発的になる可能性があります。
- 次亜塩素酸ナトリウムの希薄溶液は安定しており、家庭用漂白剤として使用されています.
- 無水 LiOCl は室温で安定ですが、NaOCl は 0 °C 以上では不安定です。
- 次亜塩素酸は分解して塩素を生成するため、単体では不安定です。
- アンモニアとの反応で、次亜塩素酸塩は次の生成物を生成します:
NH3 + ClO → H2O + NH2
NH2 Cl + ClO → HO + NHCl2
NHCl2 + ClO → H2O + NCl3
次亜塩素酸塩の使用
次亜塩素酸の重要な用途は次のとおりです。
- 有機化学で第一級アルコールをカルボン酸に酸化します。
- 次亜塩素酸塩は塩素化剤として使用されます。また、電子が豊富な芳香族炭化水素を塩素化することもできます。
- ヤコブセンのエポキシ化反応で使用され、Mn (III) を Mn (V) に変換します。
- 強力な酸化剤でもあります。
- 次亜塩素酸ナトリウム (NaOCl) および次亜塩素酸カルシウム [Ca(OCl)2 ] は衣服を白くするために使用されます。
- 染み抜き剤として使用されます。
- そのイオンは水処理剤として使用されます。
- NaOCl は、酪農場、水道、下水処理における消毒剤および消臭剤です。
- 次亜塩素酸塩は髪の色を明るくするために使用されます.
- HOCl は紙パルプの漂白などに使用されます。
- 家の水をきれいにするために使用されます。
- 次亜塩素酸イオンの主な用途は、消毒と漂白剤です。
- さまざまな消毒剤の主成分の 1 つです。
- 工業的には、漂白、悪臭の除去、表面の浄化などの働きがあります。
- 次亜塩素酸塩は、フェノールをクロロフェノールに変換するために使用されます。
- 次亜塩素酸ナトリウム溶液は、繊維産業で紙パルプ、リネン、綿、レーヨン、ジュートを漂白するための液体漂白剤として使用されています。
次亜塩素酸塩による健康被害
次亜塩素酸は多くの用途がありますが、非常に反応性が高く、腐食性があるため、多くの健康上の問題を引き起こします。その一部を以下に示します:
- 次亜塩素酸塩は吸入および摂取すると有毒になります。
- 目、尿分泌膜、皮膚を刺激します。
- 少量の家庭用漂白剤を摂取すると、胃腸の炎症を引き起こす可能性があります.
- 高濃度の家庭用漂白剤を摂取すると、喉、穿孔、口、胃、食道に重度の腐食性損傷、出血を引き起こし、最終的には死に至る可能性があります。
- 有機物に近づくと、爆発して炎上することがあります。
- 高濃度の次亜塩素酸溶液に触れると、皮膚に炎症、焼けるような痛み、水ぶくれができることがあります。
- その活発で反応性の高い性質は、燃焼を促進したり、爆発を引き起こしたりする可能性があります.
- 低レベルの次亜塩素酸塩に長期間さらされると、皮膚の炎症を引き起こす可能性があります.
結論
次亜塩素酸イオンは周囲の環境に非常に敏感で、ほとんどが溶液の形で安定した化合物を形成します。アルカリおよびアルカリ土類金属塩の形で存在します。次亜塩素酸ナトリウム、次亜塩素酸カルシウム、クロロ次亜塩素酸カルシウム、および次亜塩素酸は、一般的に見られる次亜塩素酸塩の形態です。主に家事の除菌剤や漂白剤として様々な用途に使用されています。さまざまな業界で、さまざまな方法で使用されています。しかし、それはまた、目の刺激、皮膚の火傷、水疱、毒性などの多くの健康被害を引き起こし、死に至る可能性があります.次亜塩素酸イオンは反応性が高いため、ガラス製、陶器製、ポリ塩化ビニール製のプラスチック製の容器で取り扱い、保管には十分注意する必要があります。また、カルシウムまたは次亜塩素酸ナトリウムを含む家庭用品は、子供の手の届かない安全な場所に保管する必要があります。
よくある質問
<強い>1.次亜塩素酸イオンは極性ですか、それとも無極性ですか?
A. ClO イオンは、対称に配置された 2 つの原子 (塩素と酸素) を含むため、無極性分子です。このため、両側で生成された双極子モーメントが互いに打ち消し合い、非極性分子になります。
<強い>2.次亜塩素酸塩を保管するためにガラス、PVC プラスチック、またはその他の特別な容器を使用する必要があるのはなぜですか?
A. 次亜塩素酸塩は反応性が高いため、ニッケル、銅、クロム、鉄、マンガン、コバルトなどの微量金属に非常に敏感です。微量金属だけでなく、次亜塩素酸塩は非常に反応性が高いため、ゴム、特定のプラスチック、ほとんどの種類の布地などの多くの素材を激しく攻撃します.したがって、特別なタイプの容器に慎重に保管されます。
<強い>3.次亜塩素酸イオンは酸ですか、それとも塩基ですか?
A. 次亜塩素酸イオン (ClO) は、水に溶解すると 1 つのプロトン (つまり、H) を受け入れるため、本質的に塩基です。その結果、次亜塩素酸 (HClO) が生成されます。そして、水溶液中でプロトンを受け入れる種は塩基性であることを知っています. ClO + H2 O → HClO + OH 次亜塩素酸 (HClO) は、次亜塩素酸イオン (ClO) の共役酸です。