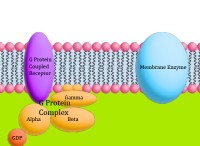
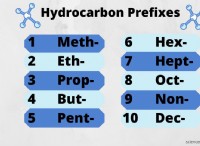
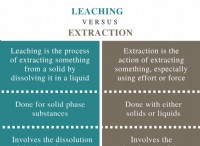
これが何が起こるかの内訳です:
* 酸: 酸には水素イオン(H+)が含まれており、pHを7未満にします。
* ベース: 塩基には水酸化物イオン(OH-)が含まれており、pHが7を超えています。
* 中和: 酸からの水素イオン(H+)は、塩基からの水酸化物イオン(OH-)と反応して水(H2O)を形成します。この反応は熱を放出し、混合物を暖かく感じさせます。
* 塩: 酸と塩基からの残りのイオンは組み合わせて塩を形成します。
例:
* 塩酸(HCl) +水酸化ナトリウム(NAOH)→塩化ナトリウム(NaCl) +水(H2O)
この反応では、酸からのH+は、塩基からOHと反応して水を形成します。残りのNa+およびcl-イオンは結合して塩を形成します。塩化ナトリウム。
覚えておくべき重要なこと:
* pHスケール: pHスケールは、溶液の酸性度または塩基性を測定します。酸はpHが低く、塩基のpHが高い。
* 熱放出: 中和反応は発熱性であり、熱を放出します。
* 塩形成: 中和反応で形成された塩は、塩基からの陽イオンと酸からの陰イオンで構成された化合物です。
酸と塩基の強度は、反応の熱放出と形成された塩に影響することに注意することが重要です。