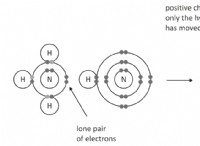
* 電子の損失: 原子が陽イオンになるために電子を失うと、それは電子シェル全体またはその一部を失います。 この損失は、原子内の全体的な電子電子反発を減らします。
* 核電荷の増加: 核内の陽子の数は同じままですが、電子が少ないと、有効な核電荷(核と残りの電子の間の引力)が増加します。
* より強いアトラクション: 核と残りの電子の間のより強い引力は、それらを核に近づけ、陽イオンを中性原子よりも小さくします。
例:
ナトリウム(Na)は、ナトリウムイオン(Na+)よりも大きな原子半径を持っています。ナトリウムが外側の電子を失うと陽イオンを形成すると、最も外側のシェル全体を失い、サイズが小さくなります。