その理由は次のとおりです。
* 価電子: これらは、原子の最も外側のエネルギーレベル(シェル)の電子です。彼らは核から最も遠いものであり、正の核の最も弱い魅力を経験します。
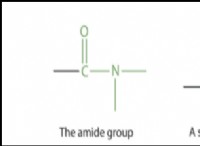
* 結合: 化学結合は、原子間の電子の共有または伝達によって形成されます。
* なぜ原子価電子: 価電子はゆるく保持されているため、他の原子との相互作用に簡単に関与し、化学結合の主要な参加者になります。
例:
*1s²2s²2pp²の電子構成を持つ炭素原子(c)を検討してください。 2S²および2p²の電子は価電子であり、これらは炭素が他の原子との結合を形成するために使用するものです。
重要な注意: 原子の原子価の数は、その化学反応性とそれが形成できる結合の種類を決定します。