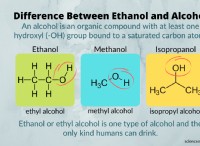
1。原子価電子数:
*炭素(c):4価電子x 2 =8
*水素(H):1価電子x 4 =4
*酸素(O):6価電子x 2 =12
*総価電子=8 + 4 + 12 =24
2。中心原子を決定します:
*炭素は最小電気陰性原子であり、分子のバックボーンを形成します。
3。原子を単一結合で接続:
* 2つの炭素を単一の結合で接続します。
*各炭素を3つの水素に接続します。
*二重結合(c =o)で1つの炭素を1つの酸素に接続します。
*他の炭素を単一の結合(C-O)で1つの酸素に接続します。
*酸素を単一の結合で水素(O-H)に接続します。
4。完全なオクテット:
*残りの電子を酸素原子の周りに孤独なペアとして分配して、オクテットを完成させます。
酢酸のLewisドット構造(Ch₃Cooh):
`` `
h o
\ //
C-C
/ \
h h
|
o
||
h
`` `
説明:
*各炭素原子は4つの原子電子を共有して4つの結合を形成します。
*各水素原子は、1つの原子電子を共有して、単一の結合を形成します。
*各酸素原子には、オクテットを完成させるために2つの孤立した電子ペアがあります。
重要な注意:
*ルイスドット構造は単純化された表現であり、分子の実際の3D構造を示していません。
*酢酸は、カルボキシル基(COOH)の存在により、水素結合を形成できます。
*酢の酸性の性質は、カルボキシル基から解離できる水素イオン(H+)に由来します。