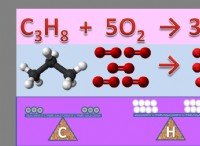
これがバランスの取れた化学式です:
3 Hcl(aq) + zn3(po4)2(s)→3 zncl2(aq) + 2 h3po4(aq)
これが何が起こるかの内訳です:
* 塩酸(HCl) 強酸であり、それは水素イオン(H+)を容易に寄付することを意味します。
* リン酸亜鉛(Zn3(PO4)2) 水に不溶性のイオン化合物です。
*塩酸からの水素イオンは、リン酸亜鉛のリン酸イオン(PO4^3-)と反応します。
*この反応は、リン酸(H3PO4)、弱酸、可溶性イオン化合物である塩化亜鉛(ZnCl2)を形成します。
全体的な反応は発熱性であり、熱を放出します。反応は完了まで進行します。つまり、リン酸亜鉛のほとんどは塩酸と反応し、塩化亜鉛とリン酸を溶液中に形成します。
注: 反応物の濃度や温度などの要因により、実際の反応が常に完了するとは限りません。