so₂(g) +no₂(g)⇌(g) + no(g)
この反応は、二酸化硫黄(SO₂)および二酸化窒素(no₂)からの三酸化硫黄(so₃)および一酸化窒素(no)の形成です 。
残念ながら、この反応の平衡定数(k)の特定の数値を提供することはできません。その理由は次のとおりです。
* 平衡定数は温度依存性です。 kの値は温度で変化します。 平衡定数を知りたい温度を指定する必要があります。
* 平衡定数は、実験的に計算または測定できます。 実験データや、kを決定するために複雑な計算を実行する能力にはアクセスできません。
平衡定数を見つける方法:
1。参照ソース:で調べます 化学の教科書、ハンドブック、またはオンラインデータベースの多くの反応の平衡定数を見つけることができます。
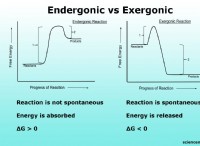
2。標準の自由エネルギー変化(Δg°)から計算: 反応の標準的な自由エネルギーの変化を知っている場合は、次の方程式を使用できます。
k =exp(-Δg°/rt)
どこ:
* kは平衡定数です
*Δg°は標準的な自由エネルギーの変化です
* rは理想的なガス定数(8.314 j/mol・k)です
* tはケルビンの温度です
この反応の温度または標準の自由エネルギーの変化があるかどうかを教えてください。平衡定数を計算するのを手伝うことができます。