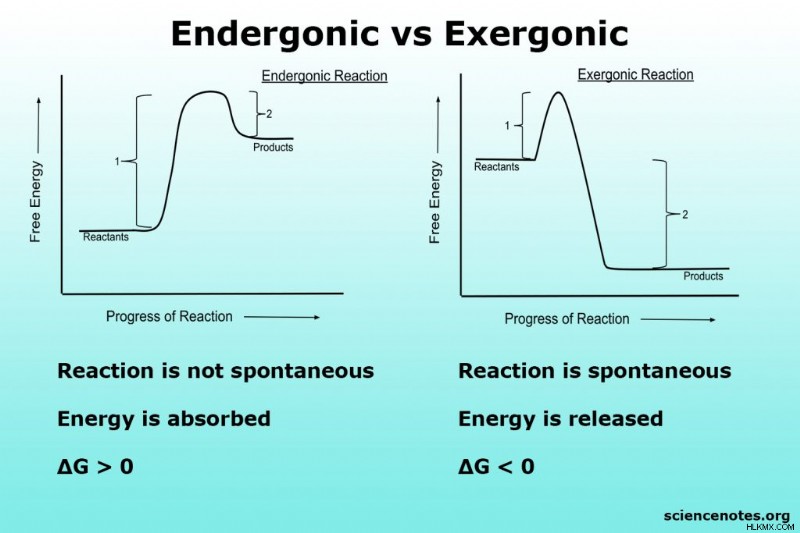
吸エルゴン反応と発エルゴン反応は、ギブスの自由エネルギーの変化に従って定義されます。吸エルゴン反応では、生成物の自由エネルギーは反応物の自由エネルギーよりも高い ((ΔG> 0; エネルギーは生成物に蓄えられる) ため、反応は自発的ではなく、生成物を作るために追加のエネルギーを供給する必要があります。反応が進行する. 発エルゴン反応では, 反応物の自由エネルギーは生成物の自由エネルギーよりも高い (ΔG <0). エネルギーは環境に放出され、反応の活性化エネルギーを克服し、自然発生的にします.
ここでは、吸エルゴン反応と発エルゴン反応、各タイプの例、および反応がどのように組み合わさって好ましくない反応が発生するかを詳しく見ていきます。
吸エルゴン反応
吸エルゴン反応は、一定の温度と圧力で、正の標準ギブス自由エネルギーを持つ化学反応です。
ΔG°> 0
言い換えれば、自由エネルギーの正味の吸収があります。製品中の化学結合がエネルギーを蓄えます。吸エルゴン反応の活性化エネルギーは通常、反応全体のエネルギーよりも大きいため、吸エルゴン反応は好ましくない反応または非自発的反応とも呼ばれます。ギブスの自由エネルギーは平衡定数、K <1 に関連するため、
好ましくない反応を進行させる方法はいくつかあります。反応を加熱したり、発エルゴン反応に結合したり、中間体を好ましい反応と共有させたりすることで、エネルギーを供給することができます。システムから製品を削除することで、反応を引き出すことができます。
吸エルゴン反応の例には、光合成、筋肉収縮と神経伝導のための Na/K ポンプ、タンパク質合成、塩化カリウムの水への溶解が含まれます。
発エルゴン反応
発エルゴン反応は、一定の温度と圧力で、負の標準ギブス自由エネルギーを持つ化学反応です:
ΔG° <0
言い換えれば、自由エネルギーの正味の放出があります。反応物内の化学結合を壊すと、製品内で新しい化学結合を形成するために使用されるエネルギーよりも多くのエネルギーが放出されます。エクセルゴニック反応は、エクセルゴニック、好ましい、または自発的な反応としても知られています。すべての反応と同様に、発エルゴン反応が進行するために供給されなければならない活性化エネルギーがあります。しかし、反応によって放出されたエネルギーは、活性化エネルギーを満たし、反応を継続させるのに十分です.発エルゴン反応は自然発生的ですが、触媒の助けがなければ迅速に進行しない場合があることに注意してください。たとえば、鉄のさびは発エルゴン的ですが、非常にゆっくりです。
発エルゴン反応の例には、細胞呼吸、過酸化水素の分解、および燃焼が含まれます。
吸エルゴン/エクエルゴン vs 吸熱/発熱
吸熱反応と発熱反応は、それぞれ吸エルゴン反応と発エルゴン反応の一種です。違いは、吸熱反応によって吸収されるエネルギーまたは発熱反応によって放出されるエネルギーが熱であることです。吸エルゴン反応と発エルゴン反応は、光や音など、熱以外のエネルギーを放出する可能性があります。たとえば、グロー スティックは、光を放出する発エルゴン反応です。熱を放出しないため、発熱反応ではありません。
正反応と逆反応
反応が一方向で吸エルゴン的である場合、それは他の方向で発エルゴン的です(逆もまた同様です)。この反応では、吸エルゴン反応と発エルゴン反応は可逆反応と呼ばれることがあります。自由エネルギーの量は順反応と逆反応で同じですが、エネルギーは吸エルゴン反応によって吸収され(正)、発エルゴン反応によって放出されます(負)。たとえば、アデノシン三リン酸 (ATP) の合成と分解を考えてみましょう。
ATP はリン酸 (Pi ) アデノシン二リン酸 (ADP) へ:
ADP + Pi → ATP + H2 〇
この反応は吸エルゴン的であり、ΔG =標準条件下で +7.3 kcal/mol。逆のプロセスである ATP の加水分解は、ギブズ自由エネルギー値の大きさが同じであるが符号が反対の -7.3 kcal/mol の発エルゴン プロセスです。
ATP + H2 O → ADP + Pi
吸エルゴン反応と発エルゴン反応の結合
化学反応は、化学平衡に達するまで順方向と逆方向の両方に進行し、順方向と逆方向の反応が同じ速度で進行します。化学平衡では、システムは最も安定したエネルギー状態にあります。
平衡は生化学にとって悪いニュースです。なぜなら、細胞は代謝反応が起こる必要があり、そうでなければ細胞は死ぬからです。細胞は、生成物と反応物の濃度を制御して、その時点で必要な反応の方向性を優先します。したがって、細胞が ATP を生成するには、エネルギーを供給して ADP を追加するか、ATP と水を除去する必要があります。 ATP をエネルギーに変換し続けるために、細胞は反応物質を供給したり、生成物を除去したりします。
多くの場合、1 つの化学反応が次の化学反応に影響を与え、吸エルゴン反応が発エルゴン反応と結合して進行するのに十分なエネルギーを与えます。たとえば、ホタルの生物発光は、ルシフェリンによる吸エルゴン発光と発エルゴン ATP 放出の結果として生じます。
参考文献
- 羽森ユージーン (2002). 「生体エネルギーの基礎を築く」 生化学および分子生物学教育 . 30 (5):296-302. doi:10.1002/bmb.2002.494030050124
- 羽森、ユージーン;ジェームズ・E・マルドリー (1984)。 「発エルゴン反応の説明に「自発的」の代わりに「熱心」という言葉を使用する」. Journal of Chemical Education . 61 (8):710. doi:10.1021/ed061p710
- IUPAC (1997)。 化学用語集 (第2版)(「ゴールドブック」)。 ISBN 0-9678550-9-8。 doi:10.1351/goldbook