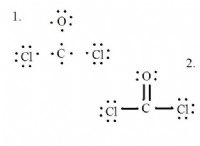* 硝酸カリウムは中性塩です。 それは、強酸(硝酸、hno₃)の反応と強い塩基(水酸化カリウム、KOH)から形成されます。水に溶解した場合、それはかなりの量のH⁺イオンを生成しません。
* pHは、h⁺イオンの濃度によって決定されます。 Kno₃のような中性塩は、pHの変化に寄与しません。
8.75のpHを達成するには、ベースを使用する必要があります。
別の塩でこのような問題にアプローチする方法は次のとおりです。
1。水中で加水分解してOH⁻イオンを生成する塩を選択します。 たとえば、弱酸(酢酸)の塩(酢酸ナトリウム)(水酸化ナトリウム)である酢酸ナトリウム(NachCooo)を使用できます。
2。必要なOH⁻の濃度を計算します。 phとpohの関係を使用できます。
* POH + pH =14
* POH =14-8.75 =5.25
* [OH⁻] =10⁻⁵.²⁵M
3。加水分解式を使用して、塩の濃度を決定します。 酢酸ナトリウムの場合、加水分解反応は次のとおりです。
*ch₃coo⁻(aq) +h₂o(l)⇌ch₃cooh(aq) +oh⁻(aq)
4。アイステーブルをセットアップ 希望する[Oh⁻]を生成するために必要な酢酸ナトリウムの濃度を解くために。
重要な注意: 特定の計算は、選択した塩とその加水分解定数(KB)に依存します。