イオンまたは電波結合:愛の移動(および電子)
電子電子結合としても知られるイオン結合は、2つの原子の間に形成される化学結合の一種であり、 有意に異なる電気陰性度 値。 二人の間の愛(および電子)の移転のように考えてください。
ここに故障があります:
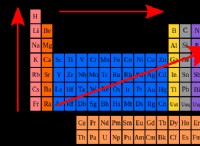
* 電気陰性度: これは、原子が化学結合に電子を引き付ける傾向です。電気陰性度が高いほど、プルが強くなります。
* 大きな違い: 2つの原子間の電気陰性度の違いが十分に大きい場合 、1つの原子は基本的に「盗み」になります もう一方の電子。
* イオン: この電子伝達により、2つのイオンが作成されます 反対の料金で:
* cation: 電子を失う原子は、積極的に帯電します 。
* アニオン: 電子を獲得する原子は、負の帯電になります 。
* 静電引力: 反対に帯電したイオンは、強い静電力を通して互いに引き付けられます 、イオン結合を形成します。
このように考えてみてください:
*ナトリウム(NA)の電気陰性度は低いため、電子を失いたいと考えています。
*塩素(CL)は高い電気陰性度を持っています。つまり、電子を獲得したいと考えています。
ナトリウムと塩素が出会うと、塩素はナトリウムから電子を「盗み」、形成します。
* na+ (陽イオンナトリウム)
* cl- (塩化物アニオン)
これらの反対に帯電したイオンは、互いに強く引き付けられ、 naCl(テーブルソルト)を形成します 。
イオン結合の重要な特性:
* strong: イオン結合は一般により強いです 共有結合よりも。
* 高融点と沸点: これは、イオン間の強い静電引力によるものです。
* 形状結晶: イオン化合物は、結晶構造を形成する傾向があります イオンの定期的な配置のため。
* 溶けたり溶解したときに電気を伝導します: イオンの自由な動きは、電気の伝導を可能にします。
イオン化合物の例:
*塩化ナトリウム(NaCl)
*臭化カリウム(KBR)
*酸化マグネシウム(MGO)
*フッ化物カルシウム(CAF2)
イオン結合のあらゆる側面の詳細についてお知らせください!