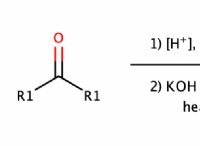
* 結合: 電子は化学結合の形成と破壊に関与しています。 原子は電子を共有または伝達して、安定した分子を作成します。
* 共有結合: 原子は電子を共有して、安定した構成を実現します。
* イオン結合: ある原子は電子を別の電子に伝達し、引き付ける反対に帯電したイオンを作成します。
* 反応性: 原子の最も外側のシェル(価電子)の電子の数は、原子の反応性を決定します。対応のない電子を持つ原子は、反応に関与する可能性が高くなります。
* エネルギー伝達: 電子はエネルギーを吸収または放出し、化学反応を促進します。
* 酸化還元反応: 電子がある原子または分子から別の原子に伝達される反応。 この移動により、多くの場合、エネルギーの放出または吸収が生じます。
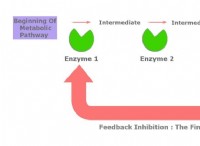
* 触媒: 酵素、生物学的触媒は、電子を使用して化学反応を促進します。彼らはしばしば一時的に電子を保持し、中間体を安定化し、反応が進むためのエネルギー障壁を下げます。
要約すると、電子は化学反応に不可欠です。なぜなら、それらは結合の形成と結合の破壊に関与し、反応性を決定し、エネルギー移動を促進するためです。
電子が化学反応にどのように関与しているかの例をいくつか紹介します。
* 燃焼: 電子は、燃料分子(炭化水素など)から酸素分子に移動し、エネルギーを熱と光として放出します。
* 光合成: 電子は、グルコースの形で光エネルギーを化学エネルギーに変換するために使用されます。
* 細胞呼吸: 電子は分子の鎖に沿って渡され、ATP、セルのエネルギー通貨を生成するために使用されるエネルギーを放出します。
化学反応における電子の役割を理解することは、最も単純な化学反応から複雑な生物学的プロセスまで、私たちの周りの世界がどのように機能するかを理解するために重要です。