1。分子構造:
* 酸性および基本官能基の両方の存在: 両性化合物には通常、陽子(酸として機能する)を寄付し、陽子(塩基として作用する)を受け入れることができる官能基が含まれています。
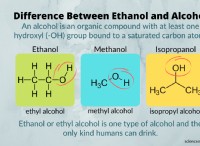
* 例: 水(H₂O)には、酸素原子に孤立した電子のペア(塩基として作用する)と、寄付できる水素原子(酸として作用する)の両方があります。 アミノ酸には、カルボキシル基(COOH、酸性)とアミノ基(NH₂、塩基性)の両方が含まれています。
* 酸性および基本的な機能グループの相対強度: 酸性および基本官能基の強度は、化合物が酸または塩基として作用する傾向に影響します。
* たとえば、 アミノ酸グリシンでは、カルボキシル基はアミノ基が塩基であるよりも強い酸です。中性溶液では、グリシンは主に酸として作用し、そのカルボキシル基からプロトンを失います。
2。反応条件:
* 溶液のpH: 周囲の溶液のpHは、両性化合物の挙動に大きく影響します。
酸性溶液中の * : 化合物は塩基として作用し、過剰なh⁺イオンを中和するために陽子を受け入れます。
* 基本ソリューション: 化合物は酸として作用し、過剰なOHイオンを中和するために陽子を寄付します。
* 反応種の性質: 両性化合物と反応する特定の化学種は、酸と塩基として機能するかどうかを決定します。
* 例: 水はHClのような強酸と反応して塩基として機能し、陽子を受け入れてh₃o⁺を形成します。また、Naohのような強い基部と反応して酸として作用し、プロトンを寄付してOH⁻を形成することもできます。
3。 平衡:
* 酸塩基平衡: 両性化合物は平衡反応に関与し、周囲の条件に応じて陽子を寄付または受け入れることができます。平衡の位置は、化合物の支配的な形態とその全体的な挙動を決定します。
要約:
両性化合物の挙動は、その分子構造、反応条件、および反応で確立された平衡の複雑な相互作用です。これは、「常に酸として行動する」または「ベースとして常に行動する」という単純なケースではなく、環境に対する動的な反応です。