1。水素結合の基本
* 水素結合とは? 水素結合は、高電気陰性原子(酸素や窒素など)に共有結合する水素原子と近くの電気陰性原子の電子ペアとの間の特別なタイプの双極子双極子相互作用です。
* 要件: 水素結合を形成するには、次のことが必要です。
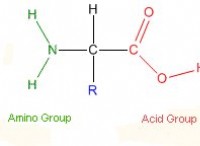
* A 水素原子 高電気陰性の原子に結合した(水やエタノール中の酸素のような)
* a 孤立ペア 別の電気陰性原子の電子の(再び、酸素のように)
2。水の構造と結合
* 酸素の2つの孤立ペア: 水(H₂O)には、その酸素原子に2つの孤立した電子のペアがあり、ドナーとして2つの水素結合を形成することができます アクセプターとしての2つの水素結合 。
3。エタノールの構造と結合
* 酸素の1つの孤独なペア: エタノール(ch₃ch₂oh)も酸素原子を持っていますが、ドナーとして1つの水素結合を形成することができる アクセプターとしての1つの水素結合 エチル基の存在のため。
4。エチル基の影響
*エタノールのエチル基(-ch₂ch₃)はかさばっていて疎水性(水補充)です。このかさばりは、水素結合の形成を妨げます。
5。結論
*水には、エタノールよりも水素結合部位が多く、水素結合形成に適した構造があります。これは、水の分子ごとに形成されたより多くの水素結合に変換されます エタノールと比較。
要約すると、酸素に2つの孤立したペアを持つ水のユニークな分子構造により、より多くの水素結合を形成し、その高い融点、沸点、および優れた溶媒としての役割に寄与します。