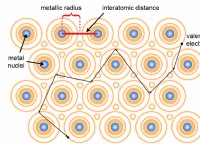
金属結合
* プロパティ:
* 熱と電気の良好な導体: 電子は非局在化されており、充電が容易になります。
* 順応性と延性: 金属格子を破壊せずに簡単に変形させることができるため、形を形作り、ワイヤーに引き込むことができます。
* 光沢: 電子は光を吸収して再放射し、光沢のある外観につながります。
* 高融点と沸点: 強力な金属結合は、壊れるために多くのエネルギーを必要とします。
* 室温で固体(水銀を除く)
* 不透明
* 例: 鉄、銅、金、アルミニウム
イオン結合
* プロパティ:
* 高融点と沸点: イオン間の強い静電魅力は、壊れるために多くのエネルギーを必要とします。
* 脆性: 応力が加えられると、イオンが変化し、反発力と破砕につながります。
* 固体状態の電気の導体が悪いが、水に溶けたり溶けたりした場合の良好な導体: イオンは固体状態の硬い格子に保持されますが、溶融または溶解すると自由に移動できます。
* 水のような極性溶媒によく溶けます: 水分子は帯電したイオンと相互作用できます。
* 結晶構造: イオンは、通常の繰り返しパターンを形成します。
* 例: 塩化ナトリウム(NaCl)、酸化マグネシウム(MGO)、炭酸カルシウム(CACO3)
共有結合
* プロパティ:
* 広範囲の融点と沸点: 共有結合のさまざまな強度。
* 室温で固体、液体、またはガスにすることができます: 結合と分子間の力の強度に依存します。
* 一般的に熱と電気の導体が貧弱: 電子は共有ペアに局在しています。
* 水への溶解度が低いことがよくあります: 非極性共有化合物は、極水分子と強く相互作用しません。
* 可変硬度と柔軟性: 共有結合の構造と強度に依存します。
* 例: 水(H2O)、メタン(CH4)、ダイヤモンド(C)、砂糖(C12H22O11)
重要なメモ:
* 中間結合: 結合が純粋に1つのタイプではなく、異なるタイプの組み合わせ(例えば、共有結合やイオン)の組み合わせである多くの物質があります。 これらの物質は、上記の特性のブレンドである特性を示すことができます。
* 例外: これらの一般的な傾向には常に例外があります。たとえば、グラファイト(共有結合を持つ純粋な炭素の形式)は、その層状構造のため、電気の優れた導体です。
これらの結合タイプまたはその特性のいずれかに深く掘り下げたい場合は、お知らせください!